Cambio de entropía
El cambio de entropía entre los estadoa a y b de un sistema está dado por
ΔS =  =
=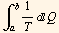
donde T es la temperatura del sistema y dQ el diferencial de calor que entra o sale de este. La integral se evalúa sobre cualquier camino reversible que conecta los dos estados. Para procesos que se dan a presión constante y la temperatura cambia de 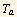 a
a 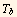 , la ecuación se puede escribir como
, la ecuación se puede escribir como
 =
=
donde 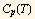 es la capacidad calorífica del sistema a presión constante.
es la capacidad calorífica del sistema a presión constante.
Determinar el cambio de temperatura para la siguiente tabla de datos se obtuvo para alguna sustancia
T (K) 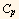 (cal/K) T (K)
(cal/K) T (K)  (cal/K)
(cal/K)
15 0.311 160 4.123
20 0.605 170 4.269
25 0.858 180 4.404
30 1.075 190 4.526
40 1.452 200 4.639
50 1.772 210 4.743
60 2.084 220 4.841
70 2.352 230 4.927
80 2.604 240 5.010
90 2.838 250 5.083
100 3.060 260 5.154
110 3.254 270 5.220
120 3.445 280 5.286
130 3.624 290 5.350
140 3.795 298.1 5.401
150 3.964
Construir una lista para los valores de temperatura en Kelvin
In[3]:=
![t = Table[i, {i, 20, 290, 10}]](../HTMLFiles/listas_263.gif)
Out[3]=
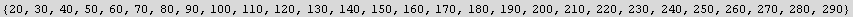
In[4]:=
![t = Prepend[t, 15]](../HTMLFiles/listas_265.gif)
Out[4]=
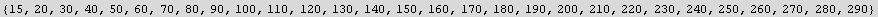
In[5]:=
![t = Insert[t, 25, 3]](../HTMLFiles/listas_267.gif)
Out[5]=
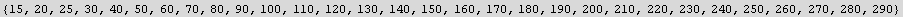
In[6]:=
![t = Append[t, 298.1]](../HTMLFiles/listas_269.gif)
Out[6]=

Construir una lista para los valores de capacidad calorífica en cal/K
In[28]:=
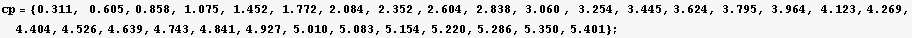
Aproximamos la integral utilizando la regla del trapecio
![Underoverscript[∑, i = 1, arg3] (C_p(T_ (i + 1))/T_ (i + 1) + C_p(T_i)/T_i) ((T_ (i + 1) - T_i)/2)](../HTMLFiles/listas_272.gif)
In[29]:=
![Underoverscript[∑, i = 1, arg3] ((t[[i + 1]] - t[[i]])/2 (cp[[i + 1]]/t[[i + 1]] + cp[[i]]/t[[i]]))](../HTMLFiles/listas_273.gif)
Out[29]=

Podemos utilizar una función de un paquete para hacer integración numérica
In[12]:=
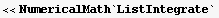
In[13]:=

![ListIntegrate[{y0, y1, ..., yn}, h, k] uses an InterpolatingFunction object of order k to give ... , you may be better off performing Integrate on the result of Fit applied to the data. More…](../HTMLFiles/listas_277.gif)
In[30]:=
![ListIntegrate[Transpose[{t, cp/t}], 1] (*lineal*)](../HTMLFiles/listas_278.gif)
Out[30]=
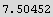
In[31]:=
![ListIntegrate[Transpose[{t, cp/t}]] (*cúbico*)](../HTMLFiles/listas_280.gif)
Out[31]=


In[26]:=

![ListPlot[{y1, y2, ... }] plots a list of values. The x coordinates for each point are taken to ... {{x1, y1}, {x2, y2}, ... }] plots a list of values with specified x and y coordinates. More…](../HTMLFiles/listas_284.gif)
In[32]:=
![ListPlot[Transpose[{t, cp}]] ;](../HTMLFiles/listas_285.gif)
![[Graphics:../HTMLFiles/listas_286.gif]](../HTMLFiles/listas_286.gif)
In[34]:=

Created by
Mathematica
(August 6, 2004)
![Underoverscript[∑, i = 1, arg3] (C_p(T_ (i + 1))/T_ (i + 1) + C_p(T_i)/T_i) ((T_ (i + 1) - T_i)/2)](../HTMLFiles/listas_272.gif)
![ListIntegrate[{y0, y1, ..., yn}, h, k] uses an InterpolatingFunction object of order k to give ... , you may be better off performing Integrate on the result of Fit applied to the data. More…](../HTMLFiles/listas_277.gif)
![[Graphics:../HTMLFiles/listas_286.gif]](../HTMLFiles/listas_286.gif)